Cátedra de Biología Celular y Molecular
BIOLOGÍA CELULAR
UNIDAD
Y DIVERSIDAD
EN
LA MATERIA VIVA
OBTENIDO DE: BIOLOGÍA MOLECULAR DE GERALD KARP,CONCEPTOS Y EXPERIMENTOS, SEXTA EDICIÓN
Reconocimiento de las células: Robert Hooke, 1655
Células vistas por Robert Hooke en una Lámina de corcho – 1655
Estudio y
esquematización de células: Anton Van Leeuwenhoek,
1673
Estudio
y esquematización de células: Anton Van Leeuwenhoek,
1673
Identificación
del núcleo y del “protoplasma”
Síntesis
de la teoría celular
- Cada organismo vivo
está formado por una o más células.
- Los organismos vivos
más pequeños son células únicas y las células son unidades funcionales de
los organismos multicelulares.
·
Todas las células provienen de
células preexistentes.
- Diversidad celular
- Unidad celular
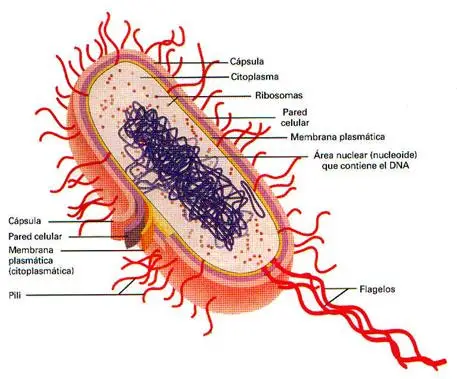
- • Membrana celular
- • Material hereditario
- • Citoplasma y orgánulos
- • De tamaño pequeño
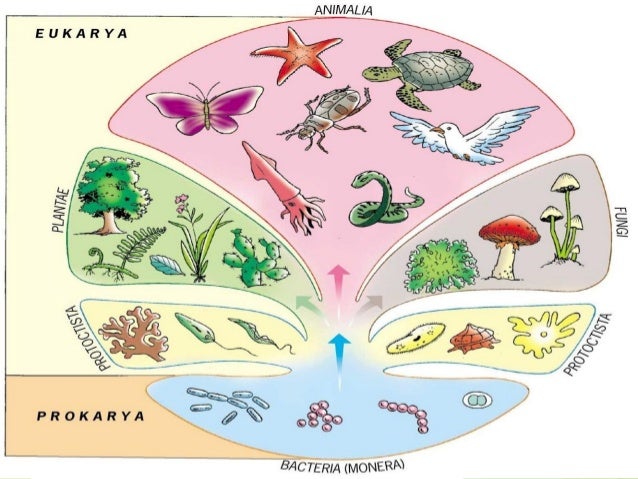
- Cinco reinos, tres células
Célula eucarionte vegetal
Célula eucarionte animal
Estructuras
de la célula eucarionte
• Núcleo
– Cromatina
– Nucléolo
• Organelos
– Retículo endoplásmico rugoso
– Retículo endoplásmico liso
– Ribosomas
– Complejo de Golgi
– Lisosomas
– Vacuolas
– Peroxisomas
– Mitocondrias
– Plastidios (célula vegetal)
• Citoesqueleto
– Microtúbulos
– Microfilamentos
– Filamentos intermedios
– Centriolos
– Cilios
– Flagelos
• Membrana plasmática
Núcleo:
Cromatina
• Contienen los Genes
R.E.R.
•
Síntesis de muchas proteínas
destinadas a la secreción o la incorporación a membranas
R.E.L.
•
Síntesis de lípidos y decodificación
de sustancias
Ribosomas
•
Síntesis de poli péptidos
(procariotas y eucariotas)
Complejo de Golgi
•
Modificación, empaque para
secreción y distribución de proteínas para otros orgánulos
Lisosomas:
•
Degradación de materiales
ingeridos, secreciones y desechos celulares
•
Catálisis de varias reacciones
metabólicas. Ejs. Degradación de H2O2 mediante la catalasa; degradación del
etanol.
Mitocondrias Respiración celular: ciclo de Krebs, transporte de electrones y fosforilación oxidativa.
Citoesqueleto: Microtúbulos, filamentos intermedios y microfilamentos
•
Estructuras sólidas, de subunidades de actina
Estructuras sólidas, de subunidades de actina
•
Soporte estructural,
movimiento celular y de orgánulos, división celular
•
Fibras resistentes estables,
formadas de polipéptidos: Ej. Miosina
•
Refuerzan cito esqueleto,
estabilizan la forma celular
•
Tubos huecos de tubulina
•
Soporte estructural,
movimiento celular y de orgánulos, división celular, en cilios, flagelos,
centriolos y cuerpos basales
Interacciones químicas.
CONCEPTO
DE NIVELES DE
ORGANIZACIÓN
Se refieren a la manera como se encuentra organizado el
protoplasma (materia viva), de
tal manera que puedan
ocurrir sobre él todos los procesos
vitales, organizados de
los simple a lo complejo
determinando el organismo.
Los niveles de organización pueden ser agrupados en tres
Categorías: químico, biológico y ecológico.
Nivel molecular
La naturaleza se rige por un principio de simplicidad molecular
El 98 % de la materia viva se forma por la combinación de 4 elementos químicos.
Sólo existen 4 tipos de biomoleculas orgánicas.
Todas las proteínas conocidas se forman por la
Combinación de 20 aminoácidos.
Todos los ADN de cualquier ser vivo se forman por la combinación de 4 tipos de nucleótidos.
BIOELEMENTOS
De los 118 elementos que se hallan en la corteza terrestre, sólo unos 25 son componentes de los seres vivos.
BIOELEMENTOS
BÁSICOS
BIOELEMENTOS
COMPLEMENTARIOS
MACROCONSTITUYENTES OLIGOELEMENTOS
Interacciones
químicas.
u
Covalente.
u No
covalente:
u Iónico.
u
Enlace
o Puente de hidrógeno.
u
Fuerzas
de Van der Waals.
u
Fuerzas
hidrófobas.
Reglas para crear una biomolecula
- Crear la
cadena de átomos de carbono (esqueleto)
- Añadir
las ramificaciones
- Añadir
los grupos funcionales
- Rellenar
con hidrógenos (“saturar”)
Precursores
de las
Macromoléculas
AMINOÁCIDOS
Los aminoácidos son cadenas carbonadas con la función ácido
(-COOH) en un carbono terminal y la función amino (-NH2), en el
Carbono
anterior (carbono )
PROPIEDADES DE LOS AMINOÁCIDOS: ÁCIDOBASE
Los aminoácidos presentan distintos
estados de ionización dependiendo
del pH:
PROPIEDADES DE LOS AMINOÁCIDOS:
ÁCIDOBASE
Cuando el pH es ácido, en el medio abundan los
protones y todos los grupos funcionales están “saturados” de H+: la carga del
aminoácido (sin tener en cuenta el radical) es (+)
PROPIEDADES
DE LOS AMINOÁCIDOS: ÁCIDOBASE
• Solubilidad alta en disolventes polares.
• Puntos de fusión elevados
(>200ºC), ya que las
atracciones
Iónicas fuertes hacen que tiendan
a cristalizar.
PROPIEDADES DE LOS AMINOÁCIDOS:
PROPIEDADES ESPACIALES
Todos los aminoácidos (menos uno)
presentan, al menos, el carbono
asimétrico, con lo que existirán
2n
isómeros
ópticos.
Por similitud con el gliceraldehído, se
denominan D-aminoácidos si tienen
el
grupo NH2 a la derecha.
En la naturaleza sólo aparecen Laminoácidos
salvo algunas bacterias y
ciertos antibióticos.
Funciones
1. Son precursores de los
péptidos y las proteínas.
2. Forman parte de vitaminas.
3. Son precursores en la síntesis
de algunas hormonas
4. Son aminoácidos, algunos
antibióticos
(cloranfenicol).
5. Algunos son metabolitos
intermediarios de
importantes vías metabólicas.
AMINOÁCIDOS NO PROTEICOS
No forman parte de proteínas,
sino que aparecen solubles, como
intermediarios metabólicos o
formando parte de las paredes



No hay comentarios:
Publicar un comentario